|
Multiple Choice
Identify the choice that best completes the statement or answers the question.
|
|
|
1.
|
Alicin adalah senyawa yang bertanggung jawab atas bau khas bawang putih. Analisis senyawa memberikan persentase komposisi massa sebagai berikut: C: 44,4%; H: 6,21%; S: 39,5%; O: 9,86 persen. Apa rumus molekul alicin jika massa molarnya sekitar 162 g/mol?
|
a.
|
C6H10S2O
|
|
b.
|
C5H10S2O
|
|
c.
|
C6H12S2O
|
|
d.
|
C7H14SO2
|
|
e.
|
C5H10S2O2
|
|
|
|
2.
|
Sampel bijih besi seberat 0,2792 g dilarutkan dalam larutan asam encer untuk mengubah seluruh besi menjadi Fe2+. Larutan tersebut memerlukan 23,30 mL 0,0194 M K2Cr2O7 untuk titrasi. Selama titrasi Cr2O72- diubah menjadi Cr3+ sedangkan Fe2+ diubah menjadi Fe3+. Berapa persentase massa besi dalam bijih tersebut?
|
a.
|
20,6%
|
|
b.
|
39,7%
|
|
c.
|
54,3%
|
|
d.
|
64,9%
|
|
e.
|
73,7%
|
|
|
|
3.
|
Pertimbangkan reaksi berikut:
2HCl(aq) + Ba(OH)2(aq) ? BaCl2(aq) + 2H2O(l) ?H = -118 kJ
Bila 100,0 mL HCl 0,500 M dicampur dengan 300,0 mL Ba(OH)2 0,100 M. Dengan asumsi suhu kedua larutan awalnya 25,0 oC dan campuran akhir mempunyai massa 400,0 g dan kalor jenis 4,18 J/oC·g, berapa suhu akhir campuran?
|
a.
|
26,8 oC
|
|
b.
|
298,15 K
|
|
c.
|
310,15 K
|
|
d.
|
30,5 oC
|
|
e.
|
20,7 oC
|
|
|
|
4.
|
Diberikan data berikut:
2NH3(g) + 3N2O(g) ? 4N2(g) + 3H2O(l) ?H = -1010 kJ
N2O(g) + 3H2(g) ? N2H4(l) + H2O(l) ?H = -317 kJ
2NH3(g) + ½O2(g) ? N2H4(l) + H2O(l) ?H = -143 kJ
H2(g) + ½O2(g) ? H2O(l) ?H = -286 kJ
Berapa nilai ?H reaksi berikut
N2H4(l) + O2(g) ? N2(g) + 2H2O(l)
|
a.
|
-125 kJ
|
|
b.
|
-250 kJ
|
|
c.
|
-465 kJ
|
|
d.
|
-576 kJ
|
|
e.
|
-623 kJ
|
|
|
|
5.
|
Jika semua reaksi berikut menyerap kalor maka reaksi yang berlangsung spontan pada suhu tinggi adalah…
I. 2H2S(g) + SO2(g) ? 3Srhombic(s) + 2H2O(g)
II. 2SO3(g) ? 2SO2(g) + O2(g)
III. Fe2O3(s) + 3H2(g) ? 2Fe(s) + 3H2O(g)
|
a.
|
I dan II
|
|
b.
|
II dan III
|
|
c.
|
I dan III
|
|
d.
|
Hanya I
|
|
e.
|
Hanya II
|
|
|
|
6.
|
Ketika elektron tereksitasi dalam atom hidrogen turun dari n = 5 ke n = 2, dipancarkan foton cahaya biru. Jika elektron tereksitasi dalam He+ turun dari n = 4, ke tingkat energi manakah elektron tersebut harus turun agar cahaya biru yang sama (seperti pada hidrogen) dapat dipancarkan?
|
|
|
7.
|
Senyawa berikut yang memiliki energi kisi paling besar adalah…
|
a.
|
CaSe
|
|
b.
|
Na2Se
|
|
c.
|
CaTe
|
|
d.
|
Na2Te
|
|
e.
|
Semua senyawa memiliki ennergi kisi yang sama.
|
|
|
|
8.
|
Perhatikan struktur Lewis berikut di mana E adalah unsur yang tidak diketahui:
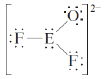
Apa kemungkinan identitas unsur E?
|
a.
|
S
|
|
b.
|
P
|
|
c.
|
Xe
|
|
d.
|
O
|
|
e.
|
Cl
|
|
|
|
9.
|
Molekul berikut yang atom pusatnya memiliki hibridisasi sp3d adalah…
|
a.
|
a, c dan e
|
|
b.
|
b dan d
|
|
c.
|
b, d dan e
|
|
d.
|
hanya d
|
|
e.
|
a dan c
|
|
|
|
10.
|
Larutan manakah yang memiliki tekanan uap tertinggi pada 28 oC?
|
a.
|
0,010 m Na3PO4 dalam air
|
|
b.
|
0,020 m CaBr2 dalam air
|
|
c.
|
0,020 m KCl dalam air
|
|
d.
|
0,020 m HF dalam air (HF adalah asam lemah.)
|
|
e.
|
0,020 m C6H12O6 dalam air.
|
|
|
|
11.
|
Sebanyak 25,00 mL sampel larutan barium nitrat 0,200 M dicampur dengan 14,00 mL larutan kalium sulfat 0,250 M. Dengan asumsi semua spesies ion terdisosiasi sempurna, berapakah tekanan osmotik campuran dalam torr?
|
a.
|
8,82 x 103 torr
|
|
b.
|
2,12 x 103 torr
|
|
c.
|
7,60 x 103 torr
|
|
d.
|
3,20 x 103 torr
|
|
e.
|
9,72 x 103 torr
|
|
|
|
12.
|
Sampel 1,60 g campuran naftalena (C10H8) dan antrasena (C14H10) dilarutkan dalam 20,0 g benzena (C6H6). Titik beku larutan adalah 2,81 oC. Berapakah persen massa naftalena dalam sampel? Titik beku benzena adalah 5,51 oC dan Kf adalah 5,12 oC·kg/mol.
|
a.
|
22%
|
|
b.
|
44%
|
|
c.
|
66%
|
|
d.
|
88%
|
|
e.
|
90%
|
|
|
|
13.
|
Pada 25oC, larutan yang mengandung karbon disulfida dan asetonitril menghasilkan tekanan total 263 torr dan 85,5 persen mol karbon disulfida pada fasa uap. Berapa fraksi mol karbon disulfida dalam larutan? Pada 25oC, tekanan uap karbon disulfida adalah 375 torr. Asumsikan larutan dan uap menunjukkan perilaku ideal.
|
a.
|
0,2
|
|
b.
|
0,3
|
|
c.
|
0,4
|
|
d.
|
0,6
|
|
e.
|
0,8
|
|
|
|
14.
|
Dekomposisi termal fosfin (PH3) menjadi fosfor dan molekul hidrogen adalah reaksi orde pertama.
4PH3(g) ? P4(g) + 6H2(g)
Waktu paruh reaksi adalah 35,0 detik pada 680°C. Berapa lama waktu yang diperlukan agar 95 persen fosfin untuk terurai?
|
a.
|
75 detik
|
|
b.
|
86 detik
|
|
c.
|
102 detik
|
|
d.
|
151 detik
|
|
e.
|
200 detik
|
|
|
|
15.
|
Diagram berikut menunjukkan perkembangan reaksi A ? B, dengan bola merah melambangkan molekul A dan bola hijau melambangkan molekul B. Berapa nilai konstanta laju reaksi tersebut?
|
a.
|
1,2883 M-1 s-1
|
|
b.
|
0,8264 s-1
|
|
c.
|
0,0347 s-1
|
|
d.
|
0,2250 M s-1
|
|
e.
|
1,8575 M-1 s-1
|
|
|
|
16.
|
Reaksi A(aq) + B(aq) ? produk(aq) dipelajari, dan diperoleh data berikut:
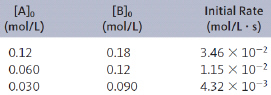
Hukum laju reaksi tersebut adalah…
|
a.
|
r = k[A][B]2
|
|
b.
|
r = k[A]2[B]
|
|
c.
|
r = k[A]
|
|
d.
|
r = k[A][B]
|
|
e.
|
r = k[B]
|
|
|
|
17.
|
Pada suhu tertentu, K = 3,75 untuk reaksi
SO2(g) + NO2(g) ? SO3(g) + NO(g)
Jika keempat gas mempunyai konsentrasi awal 0,800 M, berapa konsentrasi gas NO pada saat setimbang?
|
a.
|
1,06 M
|
|
b.
|
0,54 M
|
|
c.
|
0,26 M
|
|
d.
|
0,80 M
|
|
e.
|
1,60 M
|
|
|
|
18.
|
Reaksi penting dalam produksi hidrogen secara komersial adalah
CO(g) + H2O(g) ? H2(g) + CO2(g)
Apa yang harus dilakukan agar jumlah H2O bertambah?
|
a.
|
Menambahkan gas CO.
|
|
b.
|
Dalam wadah reaksi bervolume tetap, tekanan ditingkatkan dengan menambahkan gas helium.
|
|
c.
|
Suhu dinaikkan (reaksinya eksotermik).
|
|
d.
|
Tekanan ditingkatkan dengan mengurangi volume wadah reaksi.
|
|
e.
|
Mengeluarkan gas CO2 dari sistem kesetimbangan.
|
|
|
|
19.
|
Pada 25oC, Kp = 5,3 x 105 untuk reaksi
N2(g) + 3H2(g) ? 2NH3(g)
Ketika NH3(g) dengan tekanan tertentu dimasukkan ke dalam bejana bervolume tetap yang kosong pada suhu 25oC, kesetimbangan tercapai ketika 50,0% amonia asli telah terurai. Berapa tekanan parsial awal amonia sebelum terjadinya dekomposisi?
|
a.
|
1,2 atm
|
|
b.
|
2,1 x 10-3 atm
|
|
c.
|
4,2 x 10-2 atm
|
|
d.
|
8,4 x 10-1 atm
|
|
e.
|
6,4 x 10-3 atm
|
|
|
|
20.
|
Berapa pH larutan yang mengandung 1,0 M HF dan 1,0 M HOC6H5? (Ka HF = 7,2 x 10-4; Ka HOC6H5 = 1,6 x 10-10)
|
a.
|
1,57
|
|
b.
|
3,27
|
|
c.
|
4,75
|
|
d.
|
5,82
|
|
e.
|
6,48
|
|
|
|
21.
|
Urutan larutan 0,10 M berikut berdasarkan kenaikan pHnya adalah…
|
a.
|
NH4Br < HBr < KBr < NH3
|
|
b.
|
HBr < NH4Br < KBr < NH3
|
|
c.
|
NH4Br < KBr < HBr < NH3
|
|
d.
|
HBr < KBr < NH3 < NH4Br
|
|
e.
|
HBr < NH4Br < NH3 < KBr
|
|
|
|
22.
|
Sampel asam sebanyak 0,210 g (massa molar 5 192 g/mol) dititrasi dengan 30,5 mL NaOH 0,108 M hingga titik akhir fenolftalein. Senyawa tersebut merupakan asam…
|
a.
|
Monoprotik
|
|
b.
|
Diprotik
|
|
c.
|
Triprotik
|
|
d.
|
Tetraprotik
|
|
e.
|
Heksaprotik
|
|
|
|
23.
|
Bahan aktif aspirin adalah asam asetilsalisilat. Sampel asam asetilsalisilat seberat 2,51 g memerlukan 27,36 mL NaOH 0,5106 M untuk reaksi sempurna. Penambahan 13,68 mL HCl 0,5106 M ke dalam labu berisi aspirin dan natrium hidroksida menghasilkan campuran dengan pH = 3,48. Berapa massa molar asam asetilsalisilat dan nilai Ka-nya?
|
a.
|
180 dan 3,3 x 10-4
|
|
b.
|
120 dan 3,3 x 10-4
|
|
c.
|
180 dan 3,3 x 10-3
|
|
d.
|
120 dan 3,3 x 10-3
|
|
e.
|
150 dan 3,3 x 10-5
|
|
|
|
24.
|
Berapa massa ZnS (Ksp = 2,5 x 10-22) yang akan larut dalam 300,0 mL Zn(NO3)2 0,050 M? Abaikan sifat basa S2-.
|
a.
|
1,5 x 10-19 g
|
|
b.
|
1,5 x 10-17 g
|
|
c.
|
1,5 x 10-15 g
|
|
d.
|
1,5 x 10-13 g
|
|
e.
|
1,5 x 10-11 g
|
|
|
|
25.
|
Reaksi sel pada baterai timbal adalah
Pb(s) + PbO2(s) + 2H+(aq) + 2HSO4-(aq) ? 2PbSO4(s) + 2H2O(l)
Berapa nilai Esel pada 25oC untuk baterai ini ketika [H2SO4] = 4,5 M, yaitu, [H+] = [HSO4-] = 4,5 M? Pada 25oC, Eosel = 2,04 V untuk baterai timbal.
|
a.
|
2,04 V
|
|
b.
|
2,08 V
|
|
c.
|
2,12 V
|
|
d.
|
2,24 V
|
|
e.
|
2,50 V
|
|
|
|
26.
|
Gugus-gugus fungsi yang terdapat dalam struktur Capsaicin (menimbulkan rasa pedas pada cabe) berikut adalah…
|
a.
|
Alkena, amida, eter
|
|
b.
|
Alkena, keton, alkohol, eter
|
|
c.
|
Eter, fenol, alkena, amida
|
|
d.
|
Alkena, keton, amina, alkohol, ester
|
|
e.
|
Ester, fenol, alkena, amida
|
|
|
|
27.
|
Tata nama IUPAC yang tepat untuk senyawa berikut adalah…
|
a.
|
3-hydroxy-4-propyl-5-chloroheptane
|
|
b.
|
4-(1-chloropropyl)-3-heptanol
|
|
c.
|
4-propyl-3-chloro-5-heptanol
|
|
d.
|
4-propyl-5-chloro-3-heptanol
|
|
e.
|
5-chloro-4-propyl-3-heptanol
|
|
|
|
28.
|
Konformer yang paling stabil dari senyawa trans-1-bromo-4-metilsikloheksana adalah
|
|
|
29.
|
Hubungan antara kedua senyawa berikut adalah…
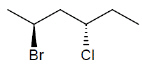
|
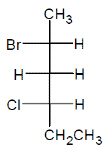
|
|
I
|
II
|
|
|
|
|
a.
|
Senyawa yang sama
|
|
b.
|
Enantiomer
|
|
c.
|
Diastereomer
|
|
d.
|
Isomer konstitusional
|
|
e.
|
Meso
|
|
|
|
30.
|
Produk utama dari reaksi berikut adalah…
|
a.
|
I dan II
|
|
b.
|
I dan IV
|
|
c.
|
Hanya III
|
|
d.
|
Hanya II
|
|
e.
|
II dan III
|
|